基因物质变化或缺陷会引起疾病发生。基因治疗是应用遗传物质和相关技术治疗各种人类疾病,由三个主要部分组成:遗传物质、用于基因传递的载体和基因编辑工具。1989年,美国国立卫生研究院进行了第一次成功的人类细胞核基因转移实验。1990年,成功为著名病人Ashanti De Silva进行了第一次基因修饰后,许多相关临床试验随之开展。然而,越来越多的失败甚至参与者死亡的事件导致了基因治疗技术的应用被停止。2006年以来,基因治疗获得多项成功实验和临床研究,这个领域的相关研究开始逐渐恢复开展。国外选择发展基因治疗,通常会考虑以下几个因素:是否是影响超过1%人口的严重疾病、是否缺乏有效的治疗方法或者当前治疗方法的成本是否过高。
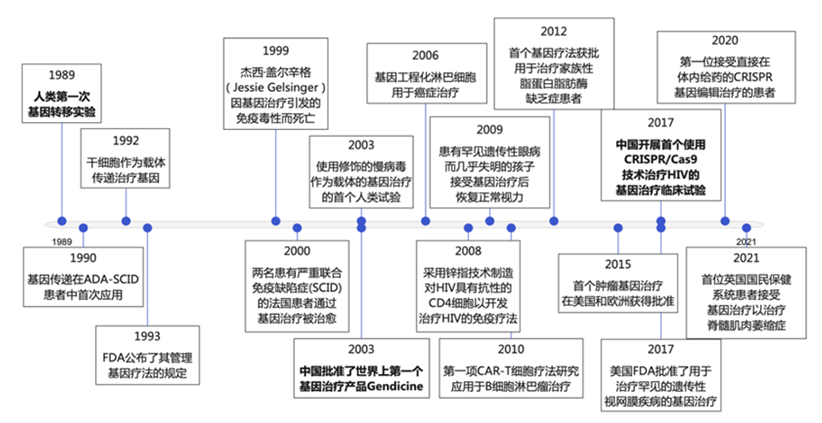
图1 基因治疗进展的时间轴(截止2021年)
01遗传物质
遗传物质可以有各种不同的形式,目前使用的遗传物质主要有以下几种:
1. 质粒:一种双链DNA分子,包含用于转录目标基因或其他遗传物质所必需的基本元素,以便对受损细胞产生影响。其具有转录起点、保守的RNA聚合酶识别位点、启动子和终止子。
2. 非编码寡核苷酸:一种由18-21个核苷酸单元组成的单链DNA分子,能够结合目标mRNA并阻止其转录。其作用机制是通过抑制RNA聚合酶功能的同时刺激核糖核酸酶H的作用,可用于治疗正常基因功能受到改变的疾病。
3. 干扰性RNA:一种单链RNA分子,能够结合到目标mRNA上,从而阻碍其转录过程,进而干扰目标基因的表达。这些分子通过干扰性RNA分子(如siRNA或miRNA)结合到RNA诱导沉默复合物(RISC)上的机制,实现对目标mRNA的调控。通常可以分为以下两种:
(1)siRNA:双链RNA的裂解会导致小干扰RNA的形成,通常具有19-21个碱基对,并结合到RISC复合物。双链的碎片化是由核酸酶3型酶Dicer的功能来完成的。RISC复合物与附着的siRNA结合到靶向mRNA并降解它。
(2)shRNA:小的发夹式RNA在茎的部分有25-29个碱基对长度,在环状区域中有4-23个碱基对长度。此链还会结合到RISC复合物以执行其功能。
02基因疗法中的载体
在基因治疗中,必须有适合的载体将遗传物质递送到身体的目标组织和细胞中。在选择适当的传递基因材料的载体时,需要考虑包括目标组织类型、基因载荷的大小以及对目标细胞的瞬时或短暂影响等条件。通常分为两类:病毒载体和非病毒载体。
1. 病毒载体
由于病毒具有感染细胞和穿透细胞膜的能力,因此病毒是基因治疗的最佳候选载体。为了使用病毒作为基因载体,它们必须在基因组中经历各种变化和修改。目前,科学家使用重组病毒技术减少它们的毒力和复制能力。
(1)逆转录病毒:一类 RNA 病毒,具有脂质包膜,每个病毒颗粒有两份单链线性正向RNA,需要长期表达治疗基因的疾病可以通过逆转录病毒治疗。
(2)慢病毒:逆转录病毒科的一类病毒,已经被改造成为基因载体,具有长期和稳定感染的著名特性,其具有两个有益的特性:它们能够传递大片段的DNA和产生最小的免疫反应。
(3)腺病毒:中等大小的病毒,含有双链DNA,具有广泛的宿主范围,在人体内不致癌,并且其基因组已完全被研究,特点在于其基因组可以轻松修改,可以产生足够数量和高浓度的重组病毒,同时可以高效表达。当需要在几天到几周的时间内实现基因表达时,腺病毒是首选的载体。
(4)腺病毒相关病毒AAV:基因物质为DNA,在人体内不会引起疾病,但与腺病毒感染有关,主要通过咽喉道途径感染人体,然后传播到身体的其他部位。一些腺病毒相关病毒会集成到人类染色体19的特定位点上,这一特点使此类腺病毒相关病毒适合作为长期表达传递的基因的载体。
(5)单纯疱疹病毒:是外周神经系统的自然寄生者,可以转化为多个转基因载体。利用其特性可以治疗外周神经系统疾病。基于单纯疱疹病毒的载体是治疗各种遗传性疾病、肿瘤、严重疼痛、自身免疫综合征、神经病理和代谢性疾病的有前途的选择。这些病毒有能够在长时间内处于潜伏期,而不对宿主细胞造成疾病或伤害的特点。HSV-1是神经系统基因传递的理想候选者,因为在感染后,这种病毒会良性地长期存在于神经元中。
(6)溶瘤病毒:基本原理是通过病毒感染并杀死癌细胞。一些病毒天生具有在肿瘤内繁殖的能力,而通过对这些自然界存在致病力较弱的病毒进行基因改造制成的特殊的溶瘤病毒,会利用靶细胞中抑癌基因的失活或缺陷从而选择性地感染肿瘤细胞,在其内大量复制并最终摧毁肿瘤细胞。此外,它还能够激活免疫系统和增强免疫反应,因此这种病毒对肿瘤的治疗效果是全面的,且不仅局限于注射部位。
(7)水痘病毒:具有包膜和双链DNA,这种病毒基因组的大小,使得其允许将大的转基因片段插入载体中进行治疗应用。用于疫苗接种的水痘病毒菌株经肿瘤内注射后,已经显示出其有望表达抗肿瘤活性。
(8)麻疹病毒:野生麻疹病毒株在人类肿瘤细胞内不会传播,但是它们的一些疫苗株具有选择性溶瘤特性。这种配体在肿瘤细胞表面高水平表达。由于此属性和对健康细胞的致病性降低,麻疹疫苗株是肿瘤治疗的适当选择。
(9)新城疫病毒:具有负链单链RNA序列,在人类中的致病性很低,只会引起轻微结膜炎。体外培养的病毒株在健康细胞中表现出降低的病原性,但它们具有相当的溶瘤活性。
2.非病毒载体
(1)脂质体:由两层脂质组成的微粒,可用于药物和基因递送的靶向治疗。脂质体可分为三个主要组:多层脂质体、小单层脂质体和大单层脂质体。
(2)聚合物:阳离子聚合物可以将带有负电荷的DNA输送到靶细胞。含有DNA的聚合物被称为聚合物复合物。迄今为止,许多聚合物已被用于基因治疗中。
(3)树状分子:一类有序的、分支状的大分子,在树枝状聚合物的合成过程中,通过添加遗传物质,DNA被捕获在大分子内,可以用于基因传递。用于基因治疗的主要聚合物是聚酰胺胺(PAMAM)。
(4)纳米颗粒:近年来,纳米粒子已被用于许多医学和生物技术应用中,例如药物开发、靶向药物输送、肿瘤治疗、消毒和卫生,以及基因治疗领域。在基因治疗中,当金、铁、胆碱、蛋白质、磷酸钙和铁硅氧化物等物质的纳米尺度颗粒用作聚合物复合物或脂质复合物的覆盖层时,通常就会被称作纳米粒子。
(5)细菌载体:基因已被证实可以从细菌转移到细胞。原核生物是很有前途的基因载体,具有相当多的优势,包括生产廉价、易于操作;在靶组织中有效增殖;可以通过给予抗生素来控制细菌的活性和复制,但也有几个缺点,比如转染率低、会激活免疫系统以及细菌细胞无法将其基因插入宿主细胞核。
03基因编辑工具
在各种基因治疗疗法中,如何操纵和编辑基因是其中的关键步骤。下面介绍几种最常用的改变基因的结构和功能的技术。
1. CRISPR‐Cas9
一种可以定点修改DNA序列的基因组编辑技术,可以用于编辑、插入或删除基因,被广泛应用于生命科学研究和基因治疗等领域。1987年,日本科学家石野良纯在细菌DNA中偶然发现的一种重复DNA结构,即CRISPR(规律间隔成簇短回文重复序列),但这些DNA重复序列的作用一直未被发现。细菌CRISPR位点最初由Francisco Mojica描述,这些片段是曾经感染过细菌的噬菌体的序列残留物。CRISPR序列在90%的古菌和约50%的细菌基因组中发现,细菌保留这些聚集的序列,并在感染期间用于检测和破坏噬菌体DNA,因此应该被认为是细菌的适应性免疫系统。Cas9是一种酶的名称,它识别CRISPR片段并在特定的裂解位点上切割它们的互补DNA。CRISPR-Cas9被用于基因组内基因编辑,成为了基因治疗非常有用和理想的工具。CRISPR-Cas9介导的基因治疗的主要组成部分是单导RNA(sgRNA),它具有一个导向序列,以定位需要修复的目标基因,并且它具有的一个框架序列可以将其固定到Cas9酶上。使用CRISPR-Cas9进行基因治疗有两种方法,第一种是通过同源重组修复(HDR)机制修复受损基因,在这个系统中,受损的靶基因通过替换为完整和健康的同源基因来进行修正;第二种是利用非同源末端连接(NHEJ)会导致DNA片段随机插入到基因序列中,从而改变基因功能或完全沉默基因的方法,用于治疗需要删除或沉默基因的遗传疾病。2018年,科学家开发了一种使用CRISPR-Cas9编辑T细胞中的自体基因的肿瘤免疫疗法,并被认为是第一个CRISPR临床试验。此后,开展了许多使用CRISPR技术的试验。
CRISPR-Cas9基因编辑技术的使用存在一些限制,主要体现在以下几个方面:
(1)脱靶效应:脱靶效应的发生率很高,在作用于目标基因时,有时也会不可避免地影响到非目标基因,导致基因组中的其他区域产生潜在的、不可预测的变化,其发生频率超过50%。
(2)需要原始空间序列相邻区域基序(PAM):PAM是Cas9进行靶向切割的必需元素,没有PAM就无法完成DNA的切割,最常用的Cas9之一是来自化脓性链球菌的SpCas9,具有短的识别位点(5’NGG3’),但由于其体积较大,因此有效地将蛋白质编码基因包装进病毒载体中具有挑战性,另一方面,SaCas9比SpCas9小,但具有更长的原始空间序列相邻区域基序(5'NNNRRT3'),这限制了该系统可以治疗的基因和遗传疾病的数量。
(3)DNA损伤毒性:编辑或敲除目标基因的第一步是通过Cas9创建切口,这往往会导致细胞凋亡并可能损伤目标组织。
2. 锌指核酸酶
锌指核酸酶是一种通过将DNA切割域和锌指融合在一起制成的限制性酶。首先,将锌指结合域改造成能够特异性结合目标基因序列。该酶会在目标序列内引发双链断裂,宿主细胞的修复机制会继续修复受损基因。与CRISPR-Cas9相比,ZNF技术较为老旧,但已用于治疗各种疾病。通过改造锌指结合域以实现特异性结合目标基因序列,ZNF技术可以用于治疗各种疾病,例如针对CCR5基因进行的靶向治疗以及治疗血友病等。ZNF技术通过腺病毒载体将ZNF编码基因传递到组织中,通过宿主细胞的修复机制修复受损基因,从而达到治疗疾病的效果。
3. 转录激活因子样效应物核酸酶
TALENs与ZNF类似,其DNA结合域是由黄单胞菌分泌的转录激活因子样效应物核酸酶组成。这些结合域是细菌的防御机制,用于抑制宿主细胞的免疫反应。TALENs最具优势的特点是可以简单地工程化它们的DNA识别位点,从而靶向所需的基因。
04基因治疗的应用进展
1.肿瘤
在肿瘤治疗中,实现满意结果的主要限制因素之一是药物耐药性。药物耐药现象即细胞在一定的药物浓度下存活的能力。在肿瘤中有两种类型的药物耐药性,一种是原发性耐药,另一种是获得性耐药。原发性耐药即肿瘤在治疗药物施用前对药物的天然抗性,而获得性耐药是指在治疗过程中,通过治疗诱导的现有癌细胞群体的遗传多样性选择而产生的。导致肿瘤获得性耐药的一个主要因素是肿瘤微环境,其由肿瘤驻留的基质细胞或生长因子组成,而这些因子会帮助癌细胞逃避治疗。由于肿瘤微环境导致的获得性耐药在免疫治疗中尤为明显。免疫抑制性肿瘤微环境,即所谓的“免疫沙漠”,被认为是肿瘤免疫治疗的最大挑战,因为其中存在髓样抑制性细胞、调节性T细胞以及肿瘤相关的细胞因子、巨噬细胞和趋化因子。克服这种情况的一些技术包括基因治疗、抗血管生成药物、溶瘤病毒、代谢调节剂或它们的组合。
克服肿瘤药物耐药性的一个重要挑战是肿瘤异质性。由于肿瘤进展或患者接受的治疗类型的改变,肿瘤异质性会逐渐演变。导致肿瘤异质性的另一个原因是基因组的不稳定性,这种现象被认为是基因治疗想要取得成功的一个主要挑战。解决这种情况的一种方法是确定癌细胞的异质性模式并靶向多个基因的组合,另一种解决方案是使用药物和基因治疗的组合治疗。肿瘤异质性也会导致肿瘤生长的不同阶段表面抗原的变化,为了克服这一障碍,研究人员设计了带有不同配体的基因治疗载体,以结合在不同生长阶段的肿瘤细胞。
基因治疗在肿瘤领域的应用潜力最为明显。例如,在肺癌模型中,基因治疗被用来通过病毒溶解、破裂和死亡的方式进行,降低癌细胞的血液供应,将基因插入癌细胞,以重新建立正常表型功能。目前,基因治疗已经在胰腺癌、肝癌和其他类型的肿瘤上进行了临床前研究,采集患者的癌细胞或可用的癌细胞系 (异体),并在体外培养。最近,肺癌和前列腺癌的基因疗法在临床试验中表现良好。“基因导向酶解药物前体治疗(GDEPT)也被用于最小化化疗的不良影响。在这种方法中,首先将表达非毒性酶的基因插入癌细胞中,然后通过系统性输送药物,该药物能够在酶的作用下转化为有毒物质,导致癌细胞死亡。例如,由单纯疱疹病毒携带的胸腺嘧啶激酶递送到肿瘤细胞中,然后通过系统性输送甘昔洛韦,在癌细胞中代谢,迫使癌细胞死亡。在过去几年中,这些基于基因治疗的分子方法发展相对较快,并可能成为未来肿瘤治疗的重要途径。
2.心血管疾病
心血管疾病(CVD)是一个普遍关注的公共卫生问题,有高昂医疗费用、临床效果不佳等问题。此外,药物诱导的心脏毒性也增加了心血管疾病的疾病负担。基因治疗将正常基因副本注入到缺陷基因的位置,从而实现疾病治疗。携带所需基因的载体通过植入引流管注射到冠状动脉、直接注射到冠状动脉或经冠状静脉通过逆行输注注入静脉系统。心衰导致肾上腺素和去甲肾上腺素在体内形成的肾上腺能受体的下调,这些受体是心衰和高血压治疗中β受体阻滞剂的靶标。心肌细胞中优势存在的腺苷酸酸化酶6(AC6)通过增强心脏的能量并升级泵功能来发挥作用,并在心衰期间降低。通过静脉注入AC6和基因治疗干预的方法可以提高AC6的表达,从而改善心功能。钙在心肌细胞的收缩和松弛机制中发挥关键作用,由SERCA2a调节。该酶活性的降低导致钙水平异常变化,引起心衰。使用基因治疗,将负责该酶的基因插入AAV1载体中,并通过静脉注射到位点进行传递,初步数据显示了心脏性能和功能状况的改善。Grossman等人用基因治疗方法治疗家族性高胆固醇血症。他们通过转导肝细胞使用逆转录病毒表达了野生型的LDL-R,即低密度脂蛋白受体。在重新植入后一年,该研究观察到总胆固醇水平从671降至608。全身基因递送也已经被探索作为治疗高胆固醇血症和高血压的基因治疗的来源。在冠心病中,基因治疗策略还可以通过微创开胸手术及外侧心脏注射进行。
3.传染性疾病
基因治疗广泛应用于那些传统临床方法无法控制的各种传染病的新型治疗方法,比如流感病毒、乙型肝炎病毒、 人乳头状瘤病毒、 疱疹单纯病毒等。用于传染病的基因治疗需要设计和插入这样的基因,这些基因可以抑制或表达基因或基因产物,在治疗中起到帮助作用。
4.神经退行性疾病:帕金森病和阿尔茨海默病
全球有大量老年人口患有神经退行性疾病。根据数据,约有580万美国人患有阿尔茨海默病痴呆,而100万美国人患有特发性帕金森病(PD)。基因治疗可以通过多种方式为患有神经退行性疾病的人提供治疗益处,例如神经修复、神经保护、直接纠正致病机制和症状控制等。在基因治疗中,通常使用病毒载体将感兴趣的基因转移、插入或传递到大脑,并在这个过程中,AAVs在临床试验中主要用于中枢神经系统疾病。对于PD,基因治疗主要采用AAV2介导的基因转移,其中包括两种治疗策略:一是谷氨酸脱羧酶(GAD)的基因转移,它负责从谷氨酸形成γ-氨基丁酸(GABA);二是一种影响多巴胺产生的速率限制酶,即芳香族L-氨基酸脱羧酶(AADC),它将左旋多巴转化为多巴胺。这个方法主要包括AAV2介导的AADC基因转移,这使得左旋多巴向多巴胺的转化速度加快。这种基因治疗方法通常会针对后交叉纹状体,因为在纹状体内,有刺状神经元在PD中不会退化,并且已经报道它们长时间表达转基因的情况。另一种作为神经修复疗法的基因治疗方法是使用GDNF和其他神经营养因子,因为它们在帕金森病的病理学方面显示出有希望的结果。
5.对遗传性疾病的基因治疗
随着对基因治疗研究的深入,纠正有缺陷基因的知识和在疾病发病过程中控制基因功能的方法也在增加。基因治疗正在使用不同的策略在治疗腺苷-脱氨酶(ADA)缺乏症、囊性纤维化、色素性视网膜炎或勒伯氏先天性黑内障、血友病、脊髓性肌萎缩等遗传性疾病方面发挥可治愈的作用。
参考文献:
1.Nilofer Sayed , Prince Allawadhi ,Gene therapy: Comprehensive overview and therapeutic applications; journal homepage: www.elsevier.com/locate/lifescience;Life Sciences 294 (2022)120375.
2.MohsenDanaeifar,Recent advances in gene therapy: genetic bullets to the root of the proble;Clinical and Experimental Medicine https://doi.org/10.1007/s10238-022-00925-x
作者:李积宗、孟海华、秦杰、冯心宜。作者单位:上海市生物医药科技发展中心。